Tropacocaína
| Tropacocaína | ||
|---|---|---|
| General | ||
| Otros nombres | benzoilpseudotropina | |
| Fórmula estructural |
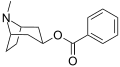 | |
| Fórmula molecular | C15H19NO2 | |
| Identificadores | ||
| Número CAS | 537-26-8[1] | |
| ChEBI | 3043 9755, 3043 | |
| ChEMBL | CHEMBL1947052 | |
| ChemSpider | 10194103 | |
| PubChem | 637578 | |
| UNII | 1I92X32F6H | |
| KEGG | C10848 | |
| Propiedades físicas | ||
| Masa molar | 245,316 9 ± 0,014 1 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La tropacocaína (TRO) (tropacaína, benzoilpseudotropina, benzoato de pseudotropina, descarbometoxicocaína) es un alcaloide del tipo tropano relacionado con la cocaína y, al igual que esta, se encuentra presente en bajas concentraciones en las plantas de la coca.[2][3] Posee una estructura similar a la de la cocaína y comparte con ella propiedades farmacológicas, destacándose por su acción como anestésico local, aunque su aplicación clínica es menos común. Se presenta generalmente como un sólido blanco cristalino, soluble en disolventes orgánicos pero con baja solubilidad en agua.[4]
Se ha encontrado tropacocaína en las siguientes especies de plantas: Erythroxylum novogranatense, E. coca, E. argentinum, E. cuneatum, E. deciduum, E. ecarinatum, E. macrocarpum, E. microphyllum, E. monogynum y E. pelleterianum.[5][6]
Historia
En 1891 el químico alemán Friedrich Giesel aisló el alcaloide tropacocaína, al que denominó benzoil-pseudotropeína, a partir de las hojas de la coca de java.[7] Posteriormente Liebermann logró sintetizar con éxito la tropacocaína, mientras que Richard Willstätter la produjo a partir de tropina.[8]
En 1892, Chadbourne lo analizó fisiológicamente, lo denominó tropacocaína e informó que:[9][8]
- La tropacocaína es mucho menos tóxica que la cocaína.
- Su efecto depresor cardíaco es menor.
- La anestesia es más completa y duradera.
- La cocaína produce isquemia, mientras que la tropacocaína produce hiperemia evanescente.
- Las soluciones de tropacocaína son ligeramente antisépticas y conservan su potencia durante al menos seis meses. Las soluciones de cocaína son menos estables, conservando su potencia durante un período mucho más corto.
- La relación entre la toxicidad y la dosis es más constante con la tropacocaína que con la cocaína.
- La recuperación de los efectos de la tropacocaína es mucho más rápida.
Importancia cultural
La tropacocaína puede ser utilizada como un marcador potencial para determinar si un individuo ha consumido hojas de coca.[3]
Síntesis
La tropocaína se puede obtener a partir de la derivatización de tropinona. Se obtiene mediante la esterificación de los ácidos correspondientes, a partir de la tropina, la cual se genera por la reducción de la tropinona.[10]
La tropacocaína se puede sintetizar a partir de la tropona en 5 etapas:[11]
- El núcleo de la tropona se trata con tetrahidroborato de sodio (NaBH4) para dar 3,5-cicloheptadien-1-ol.
- Este último reacciona con ácido benzoico en presencia de DCC, DMAP y diclorometano para dar un éster de benzoato.
- Éste se aziridiniza en uno de los dos enlaces dobles del anillo de heptadieno: esta reacción da lugar a un racémico de dos diastereoisómeros (que posteriormente darán tropacocaína o benzoiltropina).
Véase también
Referencias
- ↑ Número CAS
- ↑ Jowett, H. A. D.; Pyman, F. L. (1909). «CXVI.?Relation between chemical constitution and physiological action in the tropeines. Part II». Journal of the Chemical Society, Transactions 95: 1020-1032. doi:10.1039/CT9099501020.
- ↑ a b Cabarcos-Fernández, Pamela; Álvarez-Freire, Ivan; Rubio, Nelida Cristina; Bermejo-Barrera, Ana Maria; Moreda-Piñeiro, Antonio; Sánchez-Sellero, Ines; Tabernero-Duque, Maria Jesus (25 de enero de 2024). «Evaluation of an Oral Fluid Collection Device and a Solid-Phase Extraction Method for the Determination of Coca Leaf Alkaloids by Gas Chromatography–Mass Spectrometry». Molecules (en inglés) 29 (3): 592. ISSN 1420-3049. PMC 11154435. PMID 38338336. doi:10.3390/molecules29030592. Consultado el 24 de abril de 2025.
- ↑ «CAS 537-26-8: Tropacocaína | CymitQuimica». cymitquimica.com. Consultado el 24 de abril de 2025.
- ↑ Zuanazzi, José Angelo S.; Tremea, Valéria; Limberger, Renata P.; Sobral, Marcos; Henriques, Amélia T. (2001-08). «Alkaloids of Erythroxylum (Erythroxylaceae) species from Southern Brazil». Biochemical Systematics and Ecology (en inglés) 29 (8): 819-825. doi:10.1016/S0305-1978(01)00022-9. Consultado el 25 de abril de 2025.
- ↑ Oliveira, StenoL.; daSilva, MarceloS.; Tavares, JoseanF.; Sena‐Filho, JoséG.; Lucena, HellaneF.S.; Romero, MarcoA.V.; Barbosa‐Filho, JoséM. (2010-02). «Tropane Alkaloids from Erythroxylum Genus: Distribution and Compilation of 13 C‐NMR Spectral Data». Chemistry & Biodiversity (en inglés) 7 (2): 302-326. ISSN 1612-1872. doi:10.1002/cbdv.200800290. Consultado el 25 de abril de 2025.
- ↑ Ball, Christine; Westhorpe, Rod (2004-04). «Local Anaesthesia after Cocaine». Anaesthesia and Intensive Care (en inglés) 32 (2): 157-157. ISSN 0310-057X. doi:10.1177/0310057X0403200201. Consultado el 24 de abril de 2025.
- ↑ a b Lazarus et al., 757.
- ↑ Morrison y 1913, 1306.
- ↑ Sala Rey, Rafael; Pastor de Abram, Ana (1990). «Degradación de cocaína: alternativa para obtener derivados tropanicos». Revista de Química (PUCP) 4 (2): 138. ISSN 2518-2803. Consultado el 24 de abril de 2025.
- ↑ Chow, Winston L.; Gonzalez, Monica A.; Avanes, Arabo A.; Olson, David E. (23 de octubre de 2023). «Rapid Synthesis of Psychoplastogenic Tropane Alkaloids». JACS Au (en inglés) 3 (10): 2703-2708. ISSN 2691-3704. PMC 10598824. PMID 37885569. doi:10.1021/jacsau.3c00472. Consultado el 25 de abril de 2025.
Bibliografía
- Morrison, JTJ (21 de junio de 1913). «The Ingleby Lecture ON SPINAL ANAESTHESIA BY TROPACOCAINE; WITH A REVIEW OF 1,295 CASES: Delivered at the University of Birmingham». British Medical Journal 1 (2738): 1305-1313. PMC 2299384.
- Lazarus, Joseph A.; Pick, Chas J.; Rosenthal, Arthur A. (1933-05). «Tropacocaine Hydrochloride in Spinal Anaesthesia: Observations Based on One Thousand Operations». Annals of Surgery (en inglés) 97 (5): 757-772. ISSN 0003-4932. PMC 1391867. PMID 17866975. doi:10.1097/00000658-193305000-00012. Consultado el 25 de abril de 2025.