Cloruro de vinilideno
| Cloruro de vinilideno | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| 1,1-Dicloroeteno | ||
| General | ||
| Otros nombres |
1,1-dicloroetileno cloruro de vinilideno 1,1-DCE | |
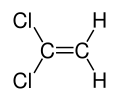
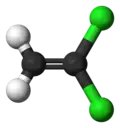
| Fórmula estructural |
 | |
| Fórmula molecular | C2H2Cl2 | |
| Identificadores | ||
| Número CAS | 75-35-4[1] | |
| Número RTECS | KV9275000 | |
| ChEMBL | CHEMBL156455 | |
| ChemSpider | 6126 | |
| UNII | 21SK105J9D | |
| KEGG | C14039 | |
| Propiedades físicas | ||
| Apariencia | Líquido incoloro | |
| Densidad | 1213 kg/m³; 1,213 g/cm³ | |
| Masa molar | 96,94 g/mol | |
| Punto de fusión | −122 °C (151 K) | |
| Punto de ebullición | 32 °C (305 K) | |
| Propiedades químicas | ||
| Momento dipolar | 1,3 D | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El 1,1-dicloroeteno, comúnmente llamado 1,1-dicloroetileno (1,1-DCE) o también cloruro de vinilideno, es un compuesto organoclorado con la fórmula molecular C2H2Cl2. El cloruro de vinilideno (VDC) es un líquido incoloro o amarillento y de olor dulzón. Como la mayoría de organoclorados, es poco soluble en agua, pero soluble en disolventes orgánicos.
Producción
El 1,1-DCE es producido por deshidrocloración del 1,1,2-tricloroetano, un subproducto relativamente no deseado en la producción del 1,1,1-tricloroetano y 1,2-dicloroetano. La conversión implica una reacción catalizada por base:
- Cl2CHCH2Cl + NaOH → Cl2C=CH2 + NaCl + H2O
La reacción en fase gas, sin la base, sería más deseable, pero es menos selectiva.[2]
Aplicaciones
El 1,1-DCE se utiliza principalmente como un comonómero en la polimerización de cloruro de vinilo, acrilonitrilo, y acrilatos. También se utiliza en la fabricación de dispositivos semiconductores para el cultivo de películas de dióxido de silicio de alta pureza (SiO2).
Cloruro de polivinilideno
Como con muchos otros alquenos, el 1,1-DCE puede polimerizar. Así forma el cloruro de polivinilideno (PVDC), un producto muy utilizado como film transparente. Durante la década de 1990 la investigación sugiere que, al igual que muchos de los compuestos de carbono clorados, estos films planteaban un posible peligro para la salud en la lixiviación, especialmente sobre la exposición a los alimentos en hornos de microondas. Poco a poco, estos films se sustituyeron en la industria alimentaria por los de polietileno actuales.
Toxicología
Estudios en animales indican que el VDC se absorbe rápidamente después de exposición inhalatoria o ingestión; no hay información sobre absorción dérmica, que no se descarta por su bajo peso molecular y su naturaleza hidrofóbica, pero no es probable, porque a temperatura corporal adopta forma gaseosa. La mayoría del VDC absorbido se metaboliza rápidamente, y el que no se metaboliza se exhala, por lo que no se produce bioacumulación significativa.[3]
Referencias
- ↑ Número CAS
- ↑ Manfred Rossberg, Wilhelm Lendle, Gerhard Pfleiderer, Adolf Tögel, Eberhard-Ludwig Dreher, Ernst Langer, Heinz Rassaerts, Peter Kleinschmidt, Heinz Strack, Richard Cook, Uwe Beck, Karl-August Lipper, Theodore R. Torkelson, Eckhard Löser, Klaus K. Beutel, Trevor Mann "Chlorinated Hydrocarbons" in Ullmann's Encyclopedia of Industrial Chemistry 2006, Wiley-VCH, Weinheim. doi 10.1002/14356007.a06_233.pub2.
- ↑ CLORURO DE VINILIDENO. DOCUMENTACIÓN TOXICOLÓGICA PARA EL ESTABLECIMIENTO DEL LÍMITE DE EXPOSICIÓN PROFESIONAL DEL CLORURO DE VINILIDENO DLEP 122 2018. https://www.insst.es/documents/94886/431980/DLEP+122++Cloruro+de+vinilideno++A%C3%B1o+2018.pdf/16549f2c-2579-4cb0-9daf-dfec93f3a992?version=1.0&t=1551310412311