Pentametilbenceno
| Pentametilbenceno | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
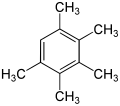
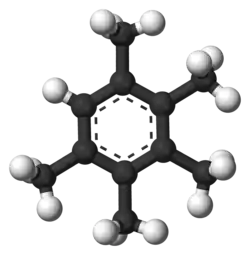
| 1,2,3,4,5-Pentametilbenceno | ||
| General | ||
| Fórmula molecular | C11H16 | |
| Identificadores | ||
| Número CAS | 700-12-9[1] | |
| ChEBI | CHEBI:38998 | |
| ChemSpider | 12259 | |
| PubChem | 12784 | |
| UNII | H6JLD3AI98 | |
| Propiedades físicas | ||
| Apariencia | Sólido incoloro | |
| Densidad | 917 kg/m³; 0,917 g/cm³ | |
| Masa molar | 148,25 g/mol | |
| Punto de fusión | 54,5 °C (328 K) | |
| Punto de ebullición | 232 °C (505 K) | |
| Peligrosidad | ||
| SGA |
  | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El pentametilbenceno es un compuesto orgánico con la fórmula C6H(CH3)5. Es un sólido incoloro con un olor dulce. El compuesto se clasifica como un hidrocarburo aromático. Es un derivado del benceno que se oxida con relativa facilidad, con E1/2 de 1,95 V frente a NHE.[2]
Síntesis y reacciones
Se obtiene como un producto menor en la metilación de Friedel-Crafts de xileno a dureno (1,2,4,5-tetrametilbenceno).[3]
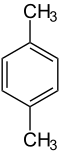 + 3CH
+ 3CH
3Cl → + 3HCl
+ 3HCl
Al igual que el dureno, el pentametilbenceno es bastante rico en electrones y sufre sustitución electrofílica fácilmente. De hecho, se utiliza como eliminador de carbocationes.[4]
Se ha observado que el pentametilbenceno es un intermedio en la formación de hexametilbenceno a partir de fenol[5] y se ha reportado que la alquilación de dureno o pentametilbenceno, al reaccionar en un entorno anhidro con clorometano y en presencia de cloruro de aluminio como catalizador, es un material de partida adecuado para la síntesis de hexametilbenceno:[3]
 + CH
+ CH
3Cl →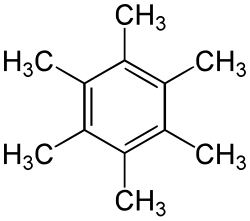 + HCl
+ HCl
Referencias
- ↑ Número CAS
- ↑ Howell, J. O.; Goncalves, J. M.; Amatore, C.; Klasinc, L.; Wightman, R. M.; Kochi, J. K. (1984). «Electron transfer from aromatic hydrocarbons and their pi-complexes with metals. Comparison of the standard oxidation potentials and vertical ionization potentials». Journal of the American Chemical Society 106 (14): 3968-3976. doi:10.1021/ja00326a014.
- ↑ a b Smith, Lee Irvin (1930). «Durene [By-products, penta- and hexamethylbenzene]». Organic Syntheses 10 (32): 248. doi:10.15227/orgsyn.010.0032.
- ↑ Okaya, Shun; Okuyama, Keiichiro; Okano, Kentaro; Tokuyama, Hidetoshi (2016). «Trichloroboron-Promoted Deprotection of Phenolic Benzyl Ether Using Pentamethylbenzene as a Non Lewis-Basic Cation Scavenger». Organic Syntheses 93: 63-74. doi:10.15227/orgsyn.093.0063.
- ↑ Landis, Phillip S.; Haag, Werner O. (1963). «Formation of Hexamethylbenzene from Phenol and Methanol». Journal of Organic Chemistry 28 (2): 585. doi:10.1021/jo01037a517.