Pentaeritritol
| Pentaeritritol | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| 2,2-Bis(hidroximetil)1,3-propanodiol | ||
| General | ||
| Otros nombres | Hercules P 6, monopentaeritritol, tetrametilolmetano, THME, PETP, pentaeritrita, Pentek, Hercules Aqualon improved technical PE-200 | |
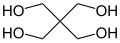
| Fórmula semidesarrollada | C(CH2OH)4 | |
| Fórmula estructural |
| |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 115-77-5[1] | |
| Número RTECS | RZ2490000 | |
| ChEBI | 134760 | |
| ChEMBL | CHEMBL3186112 | |
| ChemSpider | 7984 | |
| DrugBank | DB13526 | |
| PubChem | 8285 | |
| UNII | SU420W1S6N | |
| Propiedades físicas | ||
| Apariencia | sólido blanco | |
| Masa molar | 136,15 g/mol | |
| Punto de fusión | 533,7 K (261 °C) | |
| Punto de ebullición | 549 K (276 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | 5,6 g/100 mL a 15 °C | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El pentaeritritol es el compuesto orgánico con fórmula C(CH2OH)4. Este poliol blanco, cristalino, es un bloque de construcción versátil para la preparación de muchos compuestos polifuncionalizados, como el explosivo PENT y el triacrilato de pentaeritritol.[2] Los derivados de pentaeritritol son componentes de resinas alquídicas, barnices, PVC, ésteres del aceite de pino, y antioxidantes de olefinas.
Los ésteres de pentaeritritol libres de halógenos también son una alternativa ambientalmente amigable a los aceites de transformador, siendo tanto biodegradable como no peligroso en agua. Reemplazan ventajosamente a los policloruros de bifenilo (PCB), e incluso a los hidrocarburos fluorados basados en silicona, como fluido dieléctrico en transformadores. Su baja volatilidad y alto punto de inflamabilidad le dan una excelente resistencia a la ignición en caso de falla eléctrica mayor y ruptura del transformador.
Síntesis
Puede ser preparado por condensación del acetaldehído y el formaldehído en un medio básico.[3] El proceso ocurre por reacción aldólica sucesiva, seguida por una reacción de Cannizzaro. Las impurezas incluyen al dipentaeritritol y el tripentaeritritol.[4]
Referencias
- ↑ Número CAS
- ↑ S. F. Marrian (1948). «The Chemical Reactions of Pentaerythritol and its Derivatives». Chemical Reviews 43 (1): 149-202. doi:10.1021/cr60134a004.
- ↑ H. B. J. Schurink (1941). "Pentaerythritol". Org. Synth.; Coll. Vol. 1: 425.
- ↑ M. S. Peters, J. A. Quinn (1955). «Pentaerythritol Production Yields». Industrial & Engineering Chemistry 47 (9): 1710-1713. doi:10.1021/ie50549a016.