Oxepina
| Oxepina | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
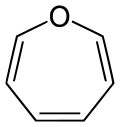
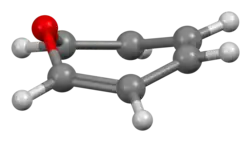
| Oxepina | ||
| General | ||
| Otros nombres | Oxacicloheptatrieno | |
| Fórmula molecular | C6H6O | |
| Identificadores | ||
| Número CAS | 291-70-3[1] | |
| ChEBI | CHEBI:230029 | |
| ChemSpider | 4953942 | |
| PubChem | 6451477 | |
| UNII | CVP5X85XX5 | |
| Propiedades físicas | ||
| Masa molar | 94,11 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La oxepina es un heterociclo que contiene oxígeno y que consiste en un anillo de siete miembros con tres enlaces dobles. El C6 H6O original existe como una mezcla en equilibrio con el óxido de benceno.
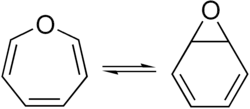
El equilibrio entre la oxepina-óxido de benceno se ve afectado por los sustituyentes del anillo.[2] Un derivado de dimetilo relacionado existe principalmente como el isómero oxepina, un líquido naranja.[3]
La oxepina es un intermediario en la oxidación del benceno por el citocromo P450 (CYP).[4] Otros óxidos de areno son metabolitos del areno original.
Síntesis
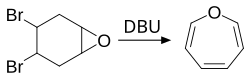
La oxepina se puede obtener mediante la reacción química del óxido de 4,5-dibromo-ciclohexeno con una base. Esta es una reacción de eliminación. Gillard y su equipo utilizó DBU como base.[5]
Referencias
- ↑ Número CAS
- ↑ Vogel, E.; Günther, H. (1967). «Benzene Oxide–Oxepin Valence Tautomerism». Angewandte Chemie International Edition in English 6 (5): 385-401. doi:10.1002/anie.196703851.
- ↑ Paquette, Leo A.; Barrett, J. H. (1969). «2,7-Dimethyloxepin». Org. Synth. 49: 62. doi:10.15227/orgsyn.049.0062.
- ↑ Snyder, R.; Witz, G.; Goldstein, B. D. (1993). «The Toxicology of Benzene». Environmental Health Perspectives 100: 293-306. PMC 1519582. PMID 8354177. doi:10.1289/ehp.93100293.
- ↑ Gillard, J. R.; Newlands, M. J.; Bridson, J. N.; Burnell, D. J. (1991). «π-Facial stereoselectivity in the Diels–Alder reactions of benzene oxides». Canadian Journal of Chemistry 69 (9): 1337-1343. doi:10.1139/v91-199.