Ortoformato de trimetilo
| Ortoformato de trimetilo | ||
|---|---|---|
| General | ||
| Fórmula estructural |
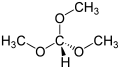 | |
| Fórmula molecular | C4H10O3 | |
| Identificadores | ||
| Número CAS | 149-73-5[1] | |
| ChEMBL | CHEMBL3187679 | |
| ChemSpider | 8655 | |
| PubChem | 9005 | |
| UNII | XAM28819YJ | |
| Propiedades físicas | ||
| Masa molar | 106,063 g/mol | |
El ortoformato de trimetilo (TMOF, por sus siglas en inglés) es un compuesto orgánico de fórmula HC(OCH3)3. Es un líquido incoloro y el ortoéster más sencillo. Es un reactivo utilizado en síntesis orgánica para la formación de éteres metílicos.[2] El producto de la reacción de un aldehído con ortoformato de trimetilo es un acetal. En general, estos acetales pueden desprotegerse de nuevo al aldehído utilizando ácido clorhídrico.
Síntesis
El ortoformato de trimetilo se prepara a escala industrial mediante la metanólisis de cianuro de hidrógeno:[3]
HCN + 3 HOCH3 → HC(OCH3)3 + NH3
El ortoformato de trimetilo también puede prepararse a partir de la reacción entre cloroformo y metóxido de sodio, un ejemplo de la síntesis del éter de Williamson.
Utilización
El ortoformato de trimetilo es un bloque de construcción útil para crear grupos metoximetileno y sistemas de anillos heterocíclicos. Introduce un grupo formilo en un sustrato nucleófilo, por ejemplo RNH2, para formar R-NH-CHO, que puede someterse a reacciones posteriores. Se utiliza en la producción de los fungicidas azoxistrobin y picoxistrobina, así como para algunos fármacos antibacterianos de la familia de la floxacina.
También se fabrican varios productos farmacéuticos intermedios a partir del ortoformato de trimetilo.[3]
El ortoformato de trimetilo también es un reactivo eficaz para convertir ácidos carboxílicos compatibles en sus correspondientes ésteres metílicos. [4]Alternativamente, las esterificaciones catalizadas por ácido con metanol pueden completarse empleando ortoformato de trimetilo para convertir el subproducto acuoso en metanol y formiato de metilo.
Referencias
- ↑ Número CAS
- ↑ Liu, Hui; Tomooka, Craig S.; Xu, Simon L.; Yerxa, Benjamin R.; Sullivan, Robert W.; Xiong, Yifeng; Moore, Harold W. (1999). «Dimethyl Squarate and ITS Conversion to 3-Ethenyl-4-Methoxycyclobutene-1,2-Dione and 2-Butyl-6-Ethenyl-5-Methoxy-1,4-Benzoquinone». Organic Syntheses 76: 189. doi:10.15227/orgsyn.076.0189.
- ↑ a b Ashford's Dictionary of Industrial Chemicals, Third edition, 2011, ISBN 978-0-9522674-3-0, page 9388
- ↑ Paine, John B. (1 de julio de 2008). «Ésteres del ácido piromelítico. Parte I. Ésteres de alcoholes aquirales: síntesis regioselectiva de ésteres de piromelitato parciales y mixtos, mecanismo de transesterificación en la esterificación cuantitativa del sistema de piromelitato utilizando ésteres de ortoformiato y una síntesis sencilla del patrón de sustitución del diéster de ortopiromelitato». The Journal of Organic Chemistry 73 (13): 4929-4938. doi:10.1021/jo800543w.
Enlaces externos
- Esta obra contiene una traducción derivada de «Trimethyl orthoformate» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.