Fluoruro de zinc
| Fluoruro de zinc | ||
|---|---|---|
 | ||
| General | ||
| Fórmula molecular | ZnF2 | |
| Identificadores | ||
| Número CAS | 7783-49-5[1] | |
| Número RTECS | ZH3200000 | |
| ChemSpider | 22957 | |
| PubChem | 10129912 24551, 10129912 | |
| UNII | L9V334775I | |
| Propiedades físicas | ||
| Masa molar | 101,926 g/mol | |
El fluoruro de zinc es un compuesto químico inorgánico con la fórmula química ZnF
2. Se encuentra en forma anhidra y también en forma de tetrahidrato, ZnF
2·4H2O (estructura cristalina romboédrica). [2] Tiene un alto punto de fusión, la estructura de rutilo y un carácter iónico apreciable en su enlace químico.[3] A diferencia de los otros haluros de zinc, ZnCl
2, ZnBr
2 y ZnI
2, no es muy soluble en agua.[3]
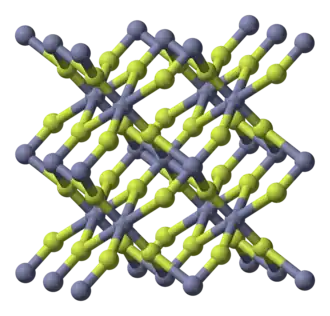
Al igual que otros difluoruros metálicos, el ZnF
2 cristaliza en la estructura rutilo, que presenta cationes Zn octaédricos y fluoruros planares trigonales.[4]
Preparación y reacciones
El fluoruro de zinc se puede sintetizar de varias maneras.
- La reacción del metal zinc con gas flúor.
- Reacción del ácido fluorhídrico con zinc, para producir gas hidrógeno (H
2) y fluoruro de zinc (ZnF
2[3]
El fluoruro de cinc puede hidrolizarse con agua caliente para formar fluoruro de hidróxido de cinc, Zn(OH)F.[5]
Se cree que la sal forma tanto un tetrahidrato como un dihidrato.[6]
Referencias
- ↑ Número CAS
- ↑ Perry, D. L.; Phillips, S. L. (1995). Handbook of Inorganic Compounds. CRC Press. ISBN 0-8493-8671-3.
- ↑ a b c Greenwood, Norman N.; Earnshaw, Alan (1997). Butterworth-Heinemann, ed. Chemistry of the Elements (2 edición). ISBN 978-0-08-037941-8.
- ↑ Stout, J. W.; Reed, Stanley A. (1954). «The Crystal Structure of MnF2, FeF2, CoF2, NiF2 and ZnF2». J. Am. Chem. Soc. 76 (21): 5279-5281. doi:10.1021/ja01650a005.
- ↑ Srivastava, O. K.; Secco, E. A. (1967). «Studies on Metal Hydroxy Compounds. I. Thermal Analyses of Zinc Derivatives ε-Zn(OH)2, Zn5(OH)8Cl2 · H2O, β-ZnOHCl, and ZnOHF». Canadian Journal of Chemistry 45 (6): 579-583. doi:10.1139/v67-096.
- ↑ Kirk-Othmer, ed. (26 de enero de 2001). Kirk-Othmer Encyclopedia of Chemical Technology (en inglés) (1 edición). Wiley. ISBN 978-0-471-48494-3. doi:10.1002/0471238961.2609140312091404.a01. Consultado el 3 de marzo de 2025.
Enlaces externos
- «Zinc Fluoride». American Elements.
- Esta obra contiene una traducción derivada de «Zinc fluoride» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.