Estructura de fluorita
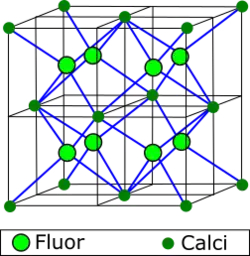
La estructura de fluorita es un modelo cristaloquímico común que define la posición en que los iones de sustancias iónicas con fórmula MX2 se colocan en la red cristalina y que tiene como origen el patrón de empaquetamiento cúbico compacto de los iones de CaF2 (fluorita). [1] En la estructura cristalina tipo fluorita, los aniones, X ocupan los ocho sitios intersticiales tetraédricos, mientras que los cationes, M, ocupan los sitios regulares de una estructura cúbica centrada en las caras (CCC). Muchos compuestos químicos cuando cristalizan adoptan esta estructura.
Por contra, muchos compuestos, de fórmula química M2X adoptan una estructura cristalina opuesta a la de la fluorita; es decir, tienen una estructura antifluorita. En estos casos, las ubicaciones de los aniones y cationes están invertidas con respecto a la fluorita; los aniones ocupan los sitios regulares del de una estructura cúbica centrada en las caras, mientras que los cationes ocupan los sitios intersticiales tetraédricos. Por ejemplo, el siliciuro de magnesio, Mg2Si, tiene un parámetro reticular de 6,338 Å con cationes de magnesio ocupando los sitios intersticiales tetraédricos, en los que cada anión de siliciuro está rodeado por ocho cationes de magnesio y cada catión de magnesio está rodeado por cuatro aniones de siliciuro de manera tetraédrica.[2]
-
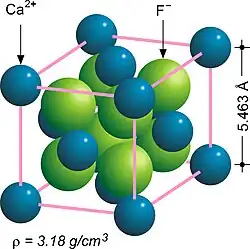 La estructura de fluorita del fluoruro de calcio CaF2 .
La estructura de fluorita del fluoruro de calcio CaF2 . -
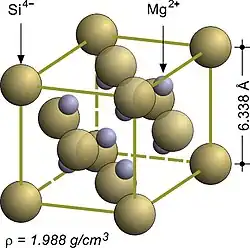 Estructura antifluorita del siliciuro de magnesio Mg2Si.
Estructura antifluorita del siliciuro de magnesio Mg2Si.
| Material | Constante de red (Å) | Estructura cristalina |
|---|---|---|
| BaF2 | 6.196 | Fluorita |
| β-PbF2 | 5,94 | Fluorita |
| PuO2 | 5.399 | Fluorita |
| SrF2 | 5.7996 | Fluorita |
| UO2 | 5.47065 | Fluorita |
| CaF2 | 5.463 | Fluorita |
| ZrO2 | 5.14 | Fluorita |
| K2O | 6.449 | Antifluorita |
| K2S | 7.406 | Antifluorita |
| Li2O | 4.61 | Antifluorita |
| Na2O | 5.55 | Antifluorita |
| Na2S | 6.54 | Antifluorita |
| Rb2O | 6,74 | Antifluorita |
| Mg2Si | 6.338 | Antifluorita |
Ejemplo de fluoruro de calcio
La cristalografía es una herramienta poderosa para investigar las estructuras de los materiales cristalinos. Es importante comprender la estructura cristalina de los materiales para formar relaciones estructura-propiedad. Estas relaciones pueden ayudar a predecir el comportamiento de los materiales cristalinos, así como introducir la capacidad de ajustar sus propiedades. El fluoruro de calcio es un ejemplo clásico de un cristal que, genéricamente, da nombre a la estructura de fluorita. La información cristalográfica se puede recopilar mediante difracción de rayos X, proporcionando información sobre las ubicaciones de la densidad de electrones dentro de una estructura cristalina. Utilizando software moderno como Olex2, [3] se puede resolver una estructura cristalina a partir de archivos de salida cristalográfica.
-
 Estructura cristalina extendida del fluoruro de calcio que muestra un cristal octaédrico.
Estructura cristalina extendida del fluoruro de calcio que muestra un cristal octaédrico.
Vistas de la estructura cristalina del fluoruro de calcio
En el fluoruro de calcio, los cationes calcio están rodeados por aniones flúor que ocupan los sitios tetraédricos, con un número de coordinación 8:4, flúor a calcio. Esta relación es consistente con la estequiometría del compuesto, donde la relación de flúor a calcio es 2:1 y se puede visualizar como una disposición cúbica de aniones que rodean los cationes de calcio.
-
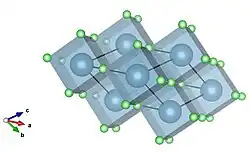 Visualización de fluoruro de calcio compartiendo esquinas cúbicas. Calcio en azul, flúor en verde.
Visualización de fluoruro de calcio compartiendo esquinas cúbicas. Calcio en azul, flúor en verde. -
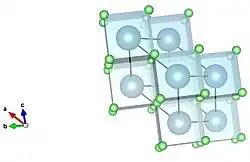 Esquina cúbica compartida visualizada desde otra pespectiva
Esquina cúbica compartida visualizada desde otra pespectiva
Estructura de fluorita extendida
Más allá de la simple celda, la estructura cristalina extendida de fluorita continúa empaquetándose en una estructura de empaquetamiento cúbico centrado en las caras (CCC (también conocida como empaquetamiento cúbico cerrado). [4] Este patrón de empaquetamiento esférico sigue un patrón ABC, donde cada capa sucesiva de esferas se asienta sobre el hueco adyacente de la red. Por el contrario, los hexagonales compactos se disponen en capas sucesivas con un patrón ABAB. Estos dos tipos de empaquetamiento son las formas más compactas de empaquetamiento esférico. [5]
-
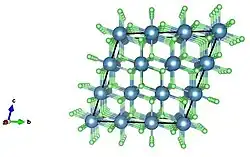 Estructura de apilamiento de cristales extendida de fluoruro de calcio; celda unitaria expandida en una unidad de 3.
Estructura de apilamiento de cristales extendida de fluoruro de calcio; celda unitaria expandida en una unidad de 3. -
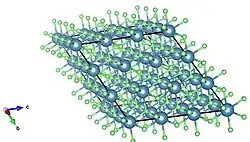 Vista de la estructura de empaquetamiento extendida del fluoruro de calcio a lo largo de un eje separado; celda unitaria expandida.
Vista de la estructura de empaquetamiento extendida del fluoruro de calcio a lo largo de un eje separado; celda unitaria expandida.
Véase también
Referencias
- ↑ Holleman, A. F., ed. (2001). Holleman-Wiberg inorganic chemistry. Academic. ISBN 978-0-12-352651-9.
- ↑ a b Rizescu, Costel; Rizescu, Mihaela (2018). Structure of Crystalline Solids, Imperfections and Defects in Crystals (en inglés) (First edición). Shutter Waves. ISBN 978-1-947641-17-4.
- ↑ «OlexSys». OlexSys.
- ↑ Shriver (January 2014). Inorganic Chemistry (Sixth edición). Oxford University Press. ISBN 978-1-4292-9906-0.
- ↑ Redwing, Ronald. «Face Centered Cubic Structure (FCC)». The Pennsylvania State University.