Cromatografía de fluidos supercríticos
La cromatografía de fluidos supercríticos también conocida como SFC (por sus siglas en inglés de Supercritical Fluid Chromatography) es una técnica de análisis cromatográfico que utiliza como fase móvil fluidos en estado supercrítico, generalmente sustancias gaseosas en condiciones normales, pero a presión y temperatura ligeramente por encima de su punto crítico.[1] En líneas generales, se puede considerar como un híbrido entre la cromatografía de gases (GC) y la cromatografía de líquidos de alta eficacia (LC o HPLC) que combina las mejores características de ambas técnicas. [2] La principal ventaja del empleo de fluidos supercríticos es que estos fluidos combinan propiedades tanto de líquidos como de gases, mejorando la capacidad eluyente y separativa de los líquidos en fase normal a la vez que ofrecen menor resistencia al paso de la fase móvil a través de la fase estacionaria, pues sus coeficientes de difusión y su viscosidad son más parecidas a las de los gases.[3] Puesto que la fase supercrítica representa un estado en el que convergen las propiedades del líquido y del gas, la cromatografía de fluidos supercríticos a veces se denomina cromatografía de convergencia,[4] [5] aunque este término no goza de gran aceptación. Se utiliza para el análisis y la purificación de moléculas de peso molecular bajo a moderado, térmicamente lábiles y también puede emplearse para la separación de compuestos quirales.
La SFC se utilizó por vez primera en 1962.[6]
Instrumentación
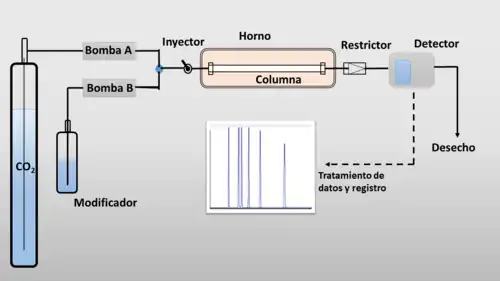
El equipo para cromatografía de fluidos supercríticos es bastante similar al que se utiliza en cromatografía líquida de alta eficacia (HPLC), pues básicamente utiliza presiones y temperaturas similares a las utilizadas en esta técnica. No obstante, existen algunas diferencias con esta técnica:[2]
- El empleo de un horno termostático capaz de albergar la columna y que permita controlar con precisión la temperatura de la fase móvil. El horno es similar al utilizado en cromatografía de gases (GC) con precisiones de décima de grado centígrado o superiores
- El uso de un restrictor, empleado para poder mantener por una parte la presión en el interior de la columna y, por otra, permitir la bajada de la presión a la salida para que el fluido supercrítico pase al estado gaseoso y pueda detectarse adecuadamente el analito. Típicamente consiste en un tubo capilar de unos 2 a 10 cm de longitud y un diámetro interno menor al de la columna (típicamente de 2 a 5 μm del diámetro), situado al final de la columna, aunque puede haber disposiciones instrumentales en las que el restrictor se coloca después de la celda de detección, dependiendo del detector utilizado.[7]
Respecto a la columna donde se produce la separación cromatográfica, esta puede contener la fase móvil empaquetada, en cuyo caso es similar en dimensiones a las utilizadas en HPLC; es decir diámetro interno entre 0,5 y 5,0 mm y un máximo de 25-30 cm de longitud, con un relleno de partícula con diámetros de 3 a 10 μm, o también, se pueden utilizar columnas capilares tubulares abiertas, de unas 50-100 μm, similares a las utilizadas en GC, aunque de longitud algo menor, de 10 a 20 m.[8] A veces, en caso de separaciones difíciles, se utilizan columnas de mayor longitud, de hasta 60 m o más.
En cuanto al procedimiento operatorio, mientras que en HPLC la fuerza eluotrópica (capacidad de elución de los solutos por el eluyente) aumenta por elución en gradiente y en cromatografía de gases por aumento de la temperatura, en la cromatografía de fluidos supercríticos, la mejora de poder eluotrópico del eluyente se consigue aumentando su densidad. Como básicamente se trata de un gas, esto se consigue aumentando la presión del sistema en el interior de la columna; es decir, en cromatografía de fluidos supercríticos habitualmente se trabaja en condiciones de gradiente de presión,[9] generalmente comenzando las eluciones mediante una primera etapa isobárica para luego aumentar la presión lineal o asintóticamente hasta el final de la elución.
Fases estacionarias
La fase estacionaria utilizada para la separación es similar a la utilizada en cromatografía líquida. Es habitual el empleo de fases ligadas unidas, por medio de polixiloxano, a las partículas de relleno o, en el caso de utilizar columnas tubulares abiertas, a la pared interna del capilar. Los espesores de las películas de fase estacionaria van desde 0,05 a 0,4 μm.
Fases móviles
La fase móvil más utilizada en la cromatografía de fluidos supercríticos es el dióxido de carbono, por tratarse de un excelente solvente de moléculas orgánicas no polares o poco polares. A ello hay que añadir la ventaja de que el CO2 se puede llevar fácilmente a condiciones supercríticas, ya que su punto crítico se alcanza a 31,3 °C y 72,9 atm de presión, que son condiciones realmente asequibles y por debajo del rango de condiciones usuales en la HPLC.
Otras propiedades que hacen que el dióxido de carbono sea un eluyente ventajoso para el empleo en este tipo de cromatografía son:
- Apolar, disuelve una gran variedad de moléculas orgánicas.
- Transparente a la radiación ultravioleta
- Inodoro
- No tóxico
- Fácil de obtener
- Barato
- No inflamable
Para ampliar el rango de analitos, puesto que el dióxido de carbono tiene carácter apolar, se le modifica con pequeñas cantidades (en torno al 1%) de solventes orgánicos polares, como el metanol y el etanol o ciertas aminas, lo que permite separar y determinar analitos polares.
Además de dióxido de carbono, también se han estudiado y alguna vez utilizado, otras fases móviles. En la siguiente tabla se indican algunas de ellas, junto con sus propiedades en el punto crítico.[8]
| Fuido | Tª crítica, ºC | P. crítica, atm | Densidad (en el punto crítico), g/mL |
|---|---|---|---|
| CO2 | 31.3 | 72,9 | 0,468 |
| N2O (óxido nitroso) | 36,5 | 71,9 | 0,457 |
| NH3 | 132,5 | 112,5 | 0,235 |
| n-butano | 152,0 | 37,5 | 0,228 |
| Dicrorodifluormetano | 111,8 | 40,7 | 0,558 |
| Dietileter | 195,6 | 35.9 | 0,265 |
Detectores
Una de las ventajas de la cromatografía de fluidos supercríticos es que en esta técnica puede emplearse el detector de ionización de llama (también usado en GC), por sus características de universalidad (permite detectar casi cualquier compuesto orgánico), alta sensibilidad y bajo mantenimiento, con la ventaja añadida de que CO2, el NH3 o el N2O utilizados como fase móvil, producen muy poca señal de fondo. El espectrómetro de masas también se puede adaptar como detector en esta técnica. También es posible adaptar a esta técnica algunos de los detectores utilizados en cromatografía líquida, como el de absorción ultravioleta o los de absorción infrarroja o los utilizados en cromatografía de gases, como el detector de conductividad térmica (TCD), el detector de captura de electrones (ACD) o el detector de fotometría de llama (FPD).[2][8] En general, los detectores adaptados de la cromatografía de gases deben modificarse para que admitan el aumento del volumen que se produce al descomprimirse el gas portador, mientras que los detectores provenientes de la cromatografía líquida, tienen que ser modificados para soportar la alta presión necesaria para mantener las condiciones supercríticas.[3] En aquellos casos en los que las variaciones de presión tienen un importante efecto sobre la señal registrada por el detector, el restrictor se coloca tras el detector, en lugar de a la salida de la columna. Esta disposición suele ser típica de los instrumentos que utilizan detectores de absorción de radiación UV. [7]
Aplicaciones
La SFC se aplica a una gran variedad de compuestos, entre los que podemos citar drogas, alimentos, herbicidas, tensioactivos, polímeros y aditivos para éstos, impelentes, explosivos o combustibles fósiles. En general, es muy adecuada para el análisis de sustancias con pesos moleculares relativamente altos, difíciles de volatilizar y, por consiguiente, difíciles de analizar mediante cromatografía de gases. Una de las aplicaciones más importantes está relacionada con las separaciones quirales de enantiómeros presentes en una mezcla racémica, de utilidad en la industria farmacéutica, ya que, por lo general, uno de los enantiómeros suele ser molécula activa, mientras que el otro, en muchos casos, puede producir efectos indeseables. En estos casos, la cromatografía de fluidos supercríticos se aplica tanto con fines analíticos como preparativos. Las mayores velocidades de difusión que pueden obtenerse mediante esta técnica, permite la obtención de picos cromatográficos con mayor resolución y más definidos, lo que permite realizar mediciones más exactas de la pureza de los enantiómeros.[2]
Véase también
Referencias
- ↑ Ettre, L. S. (1995). «1.4.04. Cromatografía de fluidos supercríticos (SFC)». En G.C.T.A. (RSEQ), ed. Nomenclatura para cromatografía. Madrid. p. 11.
- ↑ a b c d Skoog, D. A.; Holler, F. J.; . Crouch, S. R. (2008). «Cap. 29.B Cromatografía de fluidos supercríticos». Principios de análisis instrumental. Mexico: Cengage Learning. ISBN 607-481-390-6.
- ↑ a b Rubinson, Kenneth A.; Rubinson, Judith F. (2000). «Cap. 15.6. Cromatografía de fluidos supercríticos». Análisis instrumental. Prentice Hall. ISBN 84-205-2988-5.
- ↑ Waters. «Beginner's Guide to Convergence Chromatography». Consultado el 5 de junio de 2025.
- ↑ Giddings, J. Calvin; Myers, Marcus N.; McLaren, Lilian; Keller, Roy A. (4 de octubre de 1968). «High Pressure Gas Chromatography of Nonvolatile Species: Compressed gas is used to cause migration of intractable solutes.». Science (en inglés) 162 (3849): 67-73. ISSN 0036-8075. doi:10.1126/science.162.3849.67. Consultado el 5 de junio de 2025.
- ↑ Muneo Saito (2008), [1.pdf Supercritical Fluid Chromatography: A New Technology?].
- ↑ a b Rouessac, Francis; Rouessac, Annick; Rouessac, Francis; Rouessac, Francis (2000). Chemical analysis: modern instrumental methods and techniques (Engl. ed edición). Wiley. p. 98. ISBN 978-0-471-97261-7.
- ↑ a b c Kellner, Robert, ed. (1998). «Cap. 5.4 Supercritical Fluid Chromatography». Analytical chemistry: the approved text to the FECS curriculum analytical chemistry. A selection of advanced textbooks in analytical chemistry (en inglés). Wiley-VCH. ISBN 978-3-527-28881-6.
- ↑ Harris, Daniel C. (1992). Análisis Químico Cuantitativo. Grupo Editorial Iberoamericana. pp. 668-669. ISBN 970-625-003-4.