Anexo:Orbital atómico
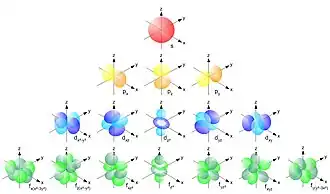
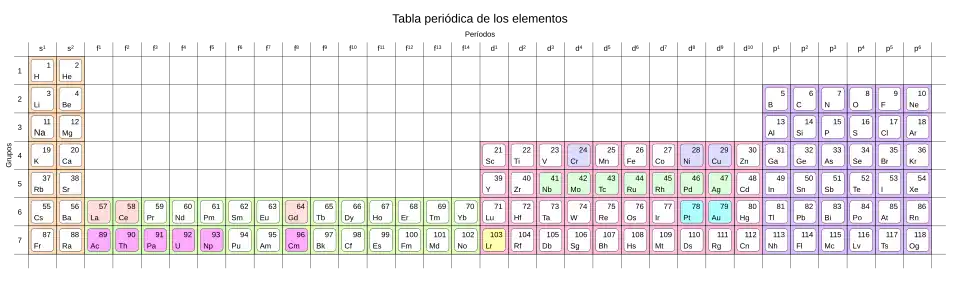
Dada tabla periódica de los elementos [1] y sus orbital atómico [2] ordenados por los número cuántico [3] así como las variaciones excepcionales que esos orbitales pueden presentar, este anexo los enumera por orden del número atómico y presenta sus características fundamentales y su estructura electrónica por: capa, orbital y número de electrones.
Diagrama de Moeller
El diagrama de Moeller, también llamado regla diagonal o regla de la sierra, es una guía utilizada para determinar la configuración electrónica de un átomo neutro a partir de su número atómico (Z). Es aplicable a la mayoría de los elementos, hay alguna excepción en los metales de transición, ya que no siempre cumplen con el principio de Aufbau.
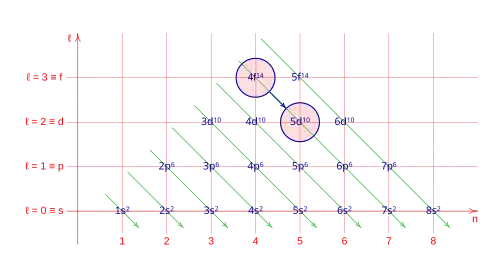
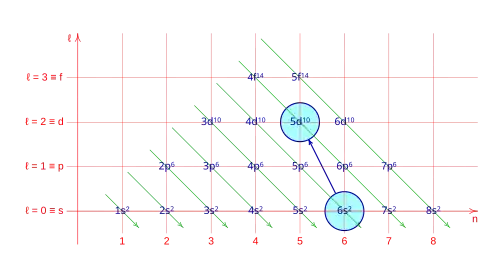
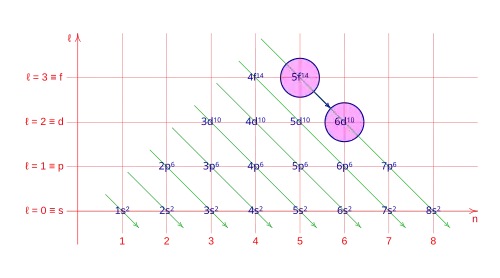
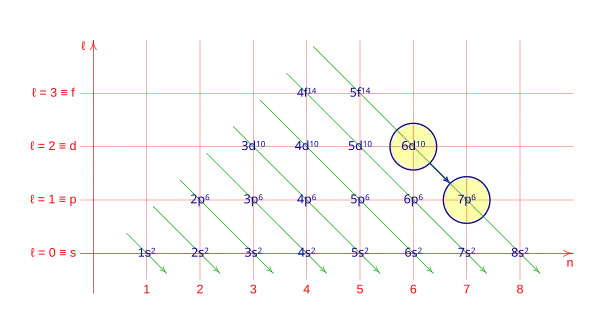
El Diagrama de Moeller es un método mnemotécnico presentado por Erwin Madelung en 1936; consiste en un gráfico en el que se escribe la configuración electrónica de los orbitales de los elementos. Se caracteriza por trazar diagonales a través de las filas y columnas del diagrama, y siguiendo la dirección de la flecha, se establece el orden de llenado de los electrones completando los orbitales de los átomos.
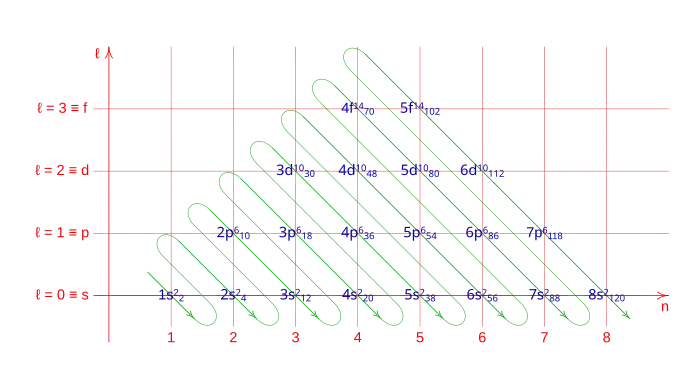
En este diagrama se pueden ver, en el eje horizontal (n) el número cuántico principal, el número de capa, en el eje vertical número cuántico azimutal (ℓ), el orbital, la flecha indica el orden con el que rellena la corteza del átomo, en cada posición se indica el número de la capa (primer número cuántico), la letra del orbital (segundo número cuántico), como superindice el número máximo de electrones que admita ese orbital, como subindice el número de electrones acumulados en el átomo hasta ese orbital inclusibe.
Aplicando este método se determina la corteza electrónica de los átomos, que se pueden ver a continuación, las excepciones se señalan expresamente.
Elementos
- Elemento: Hidrógeno
- Símbolo: H
- Periodo: 1
- Grupo: 1
- Número atómico: 1
- Orbitales para: z = 1: 1s1.
- Elemento: Helio
- Símbolo: He
- Periodo: 1
- Grupo: 18
- Número atómico: 2
- Orbitales para: z = 2: 1s2.
- Orbitales para: z = 2: [He].
- Elemento: Litio
- Símbolo: Li
- Periodo: 2
- Grupo: 1
- Número atómico: 3
- Orbitales para: z = 3: 1s2, 2s1.
- Orbitales para: z = 3: [He], 2s1.
- Elemento: Berilio
- Símbolo: Be
- Periodo: 2
- Grupo: 2
- Número atómico: 4
- Orbitales para: z = 4: 1s2, 2s2.
- Orbitales para: z = 4: [He], 2s2.
- Elemento: Boro
- Símbolo: B
- Periodo: 2
- Grupo: 13
- Número atómico: 5
- Orbitales para: z = 5: 1s2, 2s2, 2p1.
- Orbitales para: z = 5: [He], 2s2, 2p1.
- Elemento: Carbono
- Símbolo: C
- Periodo: 2
- Grupo: 14
- Número atómico: 6
- Orbitales para: z = 6: 1s2, 2s2, 2p2.
- Orbitales para: z = 6: [He], 2s2, 2p2.
- Elemento: Nitrógeno
- Símbolo: N
- Periodo: 2
- Grupo: 15
- Número atómico: 7
- Orbitales para: z = 7: 1s2, 2s2, 2p3.
- Orbitales para: z = 7: [He], 2s2, 2p3.
- Elemento: Oxígeno
- Símbolo: O
- Periodo: 2
- Grupo: 16
- Número atómico: 8
- Orbitales para: z = 8: 1s2, 2s2, 2p4.
- Orbitales para: z = 8: [He], 2s2, 2p4.
- Elemento: Flúor
- Símbolo: F
- Periodo: 2
- Grupo: 17
- Número atómico: 9
- Orbitales para: z = 9: 1s2, 2s2, 2p5.
- Orbitales para: z = 9: [He], 2s2, 2p5.
- Elemento: Neón
- Símbolo: Ne
- Periodo: 2
- Grupo: 18
- Número atómico: 10
- Orbitales para: z = 10: 1s2, 2s2, 2p6.
- Orbitales para: z = 10: [Ne].
- Elemento: Sodio
- Símbolo: Na
- Periodo: 3
- Grupo: 1
- Número atómico: 11
- Orbitales para: z = 11: 1s2, 2s2, 2p6, 3s1.
- Orbitales para: z = 11: [Ne], 3s1.
- Elemento: Magnesio
- Símbolo: Mg
- Periodo: 3
- Grupo: 2
- Número atómico: 12
- Orbitales para: z = 12: 1s2, 2s2, 2p6, 3s2.
- Orbitales para: z = 12: [Ne], 3s2.
- Elemento: Aluminio
- Símbolo: Al
- Periodo: 3
- Grupo: 13
- Número atómico: 13
- Orbitales para: z = 13: 1s2, 2s2, 2p6, 3s2, 3p1.
- Orbitales para: z = 13: [Ne], 3s2, 3p1.
- Elemento: Silicio
- Símbolo: Si
- Periodo: 3
- Grupo: 14
- Número atómico: 14
- Orbitales para: z = 14: 1s2, 2s2, 2p6, 3s2, 3p2.
- Orbitales para: z = 14: [Ne], 3s2, 3p2.
- Elemento: Fósforo
- Símbolo: P
- Periodo: 3
- Grupo: 15
- Número atómico: 15
- Orbitales para: z = 15: 1s2, 2s2, 2p6, 3s2, 3p3.
- Orbitales para: z = 15: [Ne], 3s2, 3p3.
- Elemento: Azufre
- Símbolo: S
- Periodo: 3
- Grupo: 16
- Número atómico: 16
- Orbitales para: z = 16: 1s2, 2s2, 2p6, 3s2, 3p4.
- Orbitales para: z = 16: [Ne], 3s2, 3p4.
- Elemento: Cloro
- Símbolo: Cl
- Periodo: 3
- Grupo: 17
- Número atómico: 17
- Orbitales para: z = 17: 1s2, 2s2, 2p6, 3s2, 3p5.
- Orbitales para: z = 17: [Ne], 3s2, 3p5.
- Elemento: Argón
- Símbolo: Ar
- Periodo: 3
- Grupo: 18
- Número atómico: 18
- Orbitales para: z = 18: 1s2, 2s2, 2p6, 3s2, 3p6.
- Orbitales para: z = 18: [Ar].
- Elemento: Potasio
- Símbolo: K
- Periodo: 4
- Grupo: 1
- Número atómico: 19
- Orbitales para: z = 19: 1s2, 2s2, 2p6, 3s2, 3p6, 4s1.
- Orbitales para: z = 19: [Ar], 4s1.
- Elemento: Calcio
- Símbolo: Ca
- Periodo: 4
- Grupo: 2
- Número atómico: 20
- Orbitales para: z = 20: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2.
- Orbitales para: z = 20: [Ar], 4s2.
- Elemento: Escandio
- Símbolo: Sc
- Periodo: 4
- Grupo: 3
- Número atómico: 21
- Orbitales para: z = 21: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d1.
- Orbitales para: z = 21: [Ar], 4s2, 3d1.
- Elemento: Titanio
- Símbolo: Ti
- Periodo: 4
- Grupo: 4
- Número atómico: 22
- Orbitales para: z = 22: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d2.
- Orbitales para: z = 22: [Ar], 4s2, 3d2.
- Elemento: Vanadio
- Símbolo: V
- Periodo: 4
- Grupo: 5
- Número atómico: 23
- Orbitales para: z = 23: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d3.
- Orbitales para: z = 23: [Ar], 4s2, 3d3.
- Elemento: Cromo
- Símbolo: Cr
- Periodo: 4
- Grupo: 6
- Número atómico: 24
- Orbitales para: z = 24: 1s2, 2s2, 2p6, 3s2, 3p6,
4s2, 3d4. - Orbitales para: z = 24: [Ar],
4s2, 3d4.
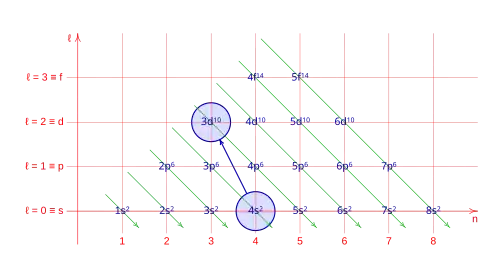
- Excepción: 1. Promoción de un electrón de 4s a 3d.
- Orbitales para: z = 24: [Ar], 4s1, 3d5.
- Elemento: Manganeso
- Símbolo: Mn
- Periodo: 4
- Grupo: 7
- Número atómico: 25
- Orbitales para: z = 25: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d5.
- Orbitales para: z = 25: [Ar], 4s2, 3d5.
- Elemento: Hierro
- Símbolo: Fe
- Periodo: 4
- Grupo: 8
- Número atómico: 26
- Orbitales para: z = 26: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d6.
- Orbitales para: z = 26: [Ar], 4s2, 3d6.
- Elemento: Cobalto
- Símbolo: Co
- Periodo: 4
- Grupo: 9
- Número atómico: 27
- Orbitales para: z = 27: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d7.
- Orbitales para: z = 27: [Ar], 4s2, 3d7.
- Elemento: Níquel

- Símbolo: Ni
- Periodo: 4
- Grupo: 10
- Número atómico: 28
- Orbitales para: z = 28: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d8.
- Orbitales para: z = 28: [Ar], 4s2, 3d8.
- En discusión: 2. Promoción de un electrón de 4s a 3d.
- Orbitales para: z = 28: [Ar], 4s1, 3d9.
- Elemento: Cobre

- Símbolo: Cu
- Periodo: 4
- Grupo: 11
- Número atómico: 29
- Orbitales para: z = 29: 1s2, 2s2, 2p6, 3s2, 3p6,
4s2, 3d9. - Orbitales para: z = 29: [Ar],
4s2, 3d9.
- Excepción: 3. Promoción de un electrón de 4s a 3d.
- Orbitales para: z = 29: [Ar], 4s1, 3d10.
- Elemento: Zinc
- Símbolo: Zn
- Periodo: 4
- Grupo: 12
- Número atómico: 30
- Orbitales para: z = 30: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10.
- Orbitales para: z = 30: [Ar], 4s2, 3d10.
- Elemento: Galio
- Símbolo: Ga
- Periodo: 4
- Grupo: 13
- Número atómico: 31
- Orbitales para: z = 31: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p1.
- Orbitales para: z = 31: [Ar], 4s2, 3d10, 4p1.
- Elemento: Germanio
- Símbolo: Ge
- Periodo: 4
- Grupo: 14
- Número atómico: 32
- Orbitales para: z = 32: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p2.
- Orbitales para: z = 32: [Ar], 4s2, 3d10, 4p2.
- Elemento: Arsénico
- Símbolo: As
- Periodo: 4
- Grupo: 15
- Número atómico: 33
- Orbitales para: z = 33: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p3.
- Orbitales para: z = 33: [Ar], 4s2, 3d10, 4p3.
- Elemento: Selenio
- Símbolo: Se
- Periodo: 4
- Grupo: 16
- Número atómico: 34
- Orbitales para: z = 34: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p4.
- Orbitales para: z = 34: [Ar], 4s2, 3d10, 4p4.
- Elemento: Bromo
- Símbolo: Br
- Periodo: 4
- Grupo: 17
- Número atómico: 35
- Orbitales para: z = 35: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p5.
- Orbitales para: z = 35: [Ar], 4s2, 3d10, 4p5.
- Elemento: Kriptón
- Símbolo: Kr
- Periodo: 4
- Grupo: 18
- Número atómico: 36
- Orbitales para: z = 36: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6.
- Orbitales para: z = 36: [Kr].
- Elemento: Rubidio
- Símbolo: Rb
- Periodo: 5
- Grupo: 1
- Número atómico: 37
- Orbitales para: z = 37: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s1.
- Orbitales para: z = 37: [Kr], 5s1.
- Elemento: Estroncio
- Símbolo: Sr
- Periodo: 5
- Grupo: 2
- Número atómico: 38
- Orbitales para: z = 38: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2.
- Orbitales para: z = 38: [Kr], 5s2.
- Elemento: Ytrio
- Símbolo: Y
- Periodo: 5
- Grupo: 3
- Número atómico: 39
- Orbitales para: z = 39: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d1.
- Orbitales para: z = 39: [Kr], 5s2, 4d1.
- Elemento: Zirconio
- Símbolo: Zr
- Periodo: 5
- Grupo: 4
- Número atómico: 40
- Orbitales para: z = 40: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d2.
- Orbitales para: z = 40: [Kr], 5s2, 4d2.
- Elemento: Niobio
- Símbolo: Nb
- Periodo: 5
- Grupo: 5
- Número atómico: 41
- Orbitales para: z = 41: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6,
5s2, 4d3. - Orbitales para: z = 41: [Kr],
5s2, 4d3.
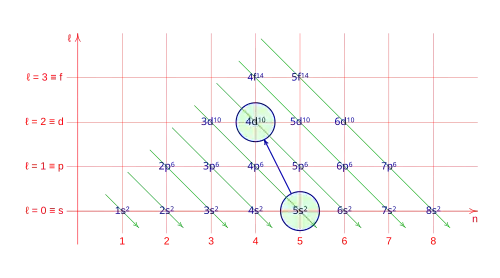
- Excepción: 4. Promoción de un electrón de 5s a 4d.
- Orbitales para: z = 41: [Kr], 5s1, 4d4.
- Elemento: Molibdeno

- Símbolo: Mo
- Periodo: 5
- Grupo: 6
- Número atómico: 42
- Orbitales para: z = 42: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6,
5s2, 4d4. - Orbitales para: z = 42: [Kr],
5s2, 4d4.
- Excepción: 5. Promoción de un electrón de 5s a 4d.
- Orbitales para: z = 42: [Kr], 5s1, 4d5.
- Elemento: Tecnecio

- Símbolo: Tc
- Periodo: 5
- Grupo: 7
- Número atómico: 43
- Orbitales para: z = 43: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6,
5s2, 4d5. - Orbitales para: z = 43: [Kr],
5s2, 4d5.
- Excepción: 6. Promoción de un electrón de 5s a 4d.
- Orbitales para: z = 43: [Kr], 5s1, 4d6.
- Elemento: Rutenio

- Símbolo: Ru
- Periodo: 5
- Grupo: 8
- Número atómico: 44
- Orbitales para: z = 44: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6,
5s2, 4d6. - Orbitales para: z = 44: [Kr],
5s2, 4d6.
- Excepción: 7. Promoción de un electrón de 5s a 4d.
- Orbitales para: z = 44: [Kr], 5s1, 4d7.
- Elemento: Rodio

- Símbolo: Rh
- Periodo: 5
- Grupo: 9
- Número atómico: 45
- Orbitales para: z = 45: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6,
5s2, 4d7. - Orbitales para: z = 45: [Kr],
5s2, 4d7.
- Excepción: 8. Promoción de un electrón de 5s a 4d.
- Orbitales para: z = 45: [Kr], 5s1, 4d8.
- Elemento: Paladio

- Símbolo: Pd
- Periodo: 5
- Grupo: 10
- Número atómico: 46
- Orbitales para: z = 46: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6,
5s2, 4d8. - Orbitales para: z = 46: [Kr],
5s2, 4d8.
- Excepción: 9. Promoción de dos electrones de 5s a 4d.
- Orbitales para: z = 46: [Kr], 5s0, 4d10.
- Elemento: Plata

- Símbolo: Ag
- Periodo: 5
- Grupo: 11
- Número atómico: 47
- Orbitales para: z = 47: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6,
5s2, 4d9. - Orbitales para: z = 47: [Kr],
5s2, 4d9.
- Excepción: 10. Promoción de un electrón de 5s a 4d.
- Orbitales para: z = 47: [Kr], 5s1, 4d10.
- Elemento: Cadmio
- Símbolo: Cd
- Periodo: 5
- Grupo: 12
- Número atómico: 48
- Orbitales para: z = 48: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10.
- Orbitales para: z = 48: [Kr], 5s2, 4d10.
- Elemento: Indio
- Símbolo: In
- Periodo: 5
- Grupo: 13
- Número atómico: 49
- Orbitales para: z = 49: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p1.
- Orbitales para: z = 49: [Kr], 5s2, 4d10, 5p1.
- Elemento: Estaño
- Símbolo: Sn
- Periodo: 5
- Grupo: 14
- Número atómico: 50
- Orbitales para: z = 50: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p2.
- Orbitales para: z = 50: [Kr], 5s2, 4d10, 5p2.
- Elemento: Antimonio
- Símbolo: Sb
- Periodo: 5
- Grupo: 15
- Número atómico: 51
- Orbitales para: z = 51: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p3.
- Orbitales para: z = 51: [Kr], 5s2, 4d10, 5p3.
- Elemento: Telurio
- Símbolo: Te
- Periodo: 5
- Grupo: 16
- Número atómico: 52
- Orbitales para: z = 52: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p4.
- Orbitales para: z = 52: [Kr], 5s2, 4d10, 5p4.
- Elemento: Yodo
- Símbolo: I
- Periodo: 5
- Grupo: 17
- Número atómico: 53
- Orbitales para: z = 53: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p5.
- Orbitales para: z = 53: [Kr], 5s2, 4d10, 5p5.
- Elemento: Xenón
- Símbolo: Xe
- Periodo: 5
- Grupo: 18
- Número atómico: 54
- Orbitales para: z = 54: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6.
- Orbitales para: z = 54: [Xe].
- Elemento: Cesio
- Símbolo: Cs
- Periodo: 6
- Grupo: 1
- Número atómico: 55
- Orbitales para: z = 55: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s1.
- Orbitales para: z = 55: [Xe], 6s1.
- Elemento: Bario
- Símbolo: Ba
- Periodo: 6
- Grupo: 2
- Número atómico: 56
- Orbitales para: z = 56: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2.
- Orbitales para: z = 56: [Xe], 6s2.
- Elemento: Lantano
- Símbolo: La
- Periodo: 6
- Grupo:
- Número atómico: 57
- Orbitales para: z = 57: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2,
4f1. - Orbitales para: z = 57: [Xe], 6s2,
4f1.
- Excepción: 11. Promoción de un electrón de 4f a 5d.
- Orbitales para: z = 57: [Xe], 6s2, 4f0, 5d1.
- Elemento: Cerio

- Símbolo: Ce
- Periodo: 6
- Grupo:
- Número atómico: 58
- Orbitales para: z = 58: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2,
4f2. - Orbitales para: z = 58: [Xe], 6s2,
4f2.
- Excepción: 12. Promoción de un electrón de 4f a 5d.
- Orbitales para: z = 58: [Xe], 6s2, 4f1, 5d1.
- Elemento: Praseodimio
- Símbolo: Pr
- Periodo: 6
- Grupo:
- Número atómico: 59
- Orbitales para: z = 59: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f3.
- Orbitales para: z = 59: [Xe], 6s2, 4f3.
- Elemento: Neodimio
- Símbolo: Nd
- Periodo: 6
- Grupo:
- Número atómico: 60
- Orbitales para: z = 60: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f4.
- Orbitales para: z = 60: [Xe], 6s2, 4f4.
- Elemento: Prometio
- Símbolo: Pm
- Periodo: 6
- Grupo:
- Número atómico: 61
- Orbitales para: z = 61: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f5.
- Orbitales para: z = 61: [Xe], 6s2, 4f5.
- Elemento: Samario
- Símbolo: Sm
- Periodo: 6
- Grupo:
- Número atómico: 62
- Orbitales para: z = 62: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f6.
- Orbitales para: z = 62: [Xe], 6s2, 4f6.
- Elemento: Europio
- Símbolo: Eu
- Periodo: 6
- Grupo:
- Número atómico: 63
- Orbitales para: z = 63: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f7.
- Orbitales para: z = 63: [Xe], 6s2, 4f7.
- Elemento: Gadolinio

- Símbolo: Gd
- Periodo: 6
- Grupo:
- Número atómico: 64
- Orbitales para: z = 64: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2,
4f8. - Orbitales para: z = 64: [Xe], 6s2,
4f8.
- Excepción: 13. Promoción de un electrón de 4f a 5d.
- Orbitales para: z = 64: [Xe], 6s2, 4f7, 5d1.
- Elemento: Terbio
- Símbolo: Tb
- Periodo: 6
- Grupo:
- Número atómico: 65
- Orbitales para: z = 65: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f9.
- Orbitales para: z = 65: [Xe], 6s2, 4f9.
- Elemento: Disprosio
- Símbolo: Dy
- Periodo: 6
- Grupo:
- Número atómico: 66
- Orbitales para: z = 66: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f10.
- Orbitales para: z = 66: [Xe], 6s2, 4f10.
- Elemento: Holmio
- Símbolo: Ho
- Periodo: 6
- Grupo:
- Número atómico: 67
- Orbitales para: z = 67: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f11.
- Orbitales para: z = 67: [Xe], 6s2, 4f11.
- Elemento: Erbio
- Símbolo: Er
- Periodo: 6
- Grupo:
- Número atómico: 68
- Orbitales para: z = 68: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f12.
- Orbitales para: z = 68: [Xe], 6s2, 4f12.
- Elemento: Tulio
- Símbolo: Tm
- Periodo: 6
- Grupo:
- Número atómico: 69
- Orbitales para: z = 69: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f13.
- Orbitales para: z = 69: [Xe], 6s2, 4f13.
- Elemento: Yterbio
- Símbolo: Yb
- Periodo: 6
- Grupo:
- Número atómico: 70
- Orbitales para: z = 70: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14.
- Orbitales para: z = 70: [Xe], 6s2, 4f14.
- Elemento: Lutecio
- Símbolo: Lu
- Periodo: 6
- Grupo: 3
- Número atómico: 71
- Orbitales para: z = 71: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d1.
- Orbitales para: z = 71: [Xe], 6s2, 4f14, 5d1.
- Elemento: Hafnio
- Símbolo: Hf
- Periodo: 6
- Grupo: 4
- Número atómico: 72
- Orbitales para: z = 72: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d2.
- Orbitales para: z = 72: [Xe], 6s2, 4f14, 5d2.
- Elemento: Tantalio
- Símbolo: Ta
- Periodo: 6
- Grupo: 5
- Número atómico: 73
- Orbitales para: z = 73: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d3.
- Orbitales para: z = 73: [Xe], 6s2, 4f14, 5d3.
- Elemento: Tungsteno
- Símbolo: W
- Periodo: 6
- Grupo: 6
- Número atómico: 74
- Orbitales para: z = 74: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d4.
- Orbitales para: z = 74: [Xe], 6s2, 4f14, 5d4.
- Elemento: Renio
- Símbolo: Re
- Periodo: 6
- Grupo: 7
- Número atómico: 75
- Orbitales para: z = 75: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d5.
- Orbitales para: z = 75: [Xe], 6s2, 4f14, 5d5.
- Elemento: Osmio
- Símbolo: Os
- Periodo: 6
- Grupo: 8
- Número atómico: 76
- Orbitales para: z = 76: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d6.
- Orbitales para: z = 76: [Xe], 6s2, 4f14, 5d6.
- Elemento: Iridio
- Símbolo: Ir
- Periodo: 6
- Grupo: 9
- Número atómico: 77
- Orbitales para: z = 77: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d7.
- Orbitales para: z = 77: [Xe], 6s2, 4f14, 5d7.
- Elemento: Platino
- Símbolo: Pt
- Periodo: 6
- Grupo: 10
- Número atómico: 78
- Orbitales para: z = 78: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6,
6s2, 4f14, 5d8. - Orbitales para: z = 78: [Xe],
6s2, 4f14, 5d8.
- Excepción: 14. Promoción de un electrón de 6s a 5d.
- Orbitales para: z = 78: [Xe], 6s1, 4f14, 5d9.
- Elemento: Oro

- Símbolo: Au
- Periodo: 6
- Grupo: 11
- Número atómico: 79
- Orbitales para: z = 79: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6,
6s2, 4f14, 5d9. - Orbitales para: z = 79: [Xe],
6s2, 4f14, 5d9.
- Excepción: 15.Promoción de un electrón de 6s a 5d.
- Orbitales para: z = 79: [Xe], 6s1, 4f14, 5d10.
- Elemento: Mercurio
- Símbolo: Hg
- Periodo: 6
- Grupo: 12
- Número atómico: 80
- Orbitales para: z = 80: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10.
- Orbitales para: z = 80: [Xe], 6s2, 4f14, 5d10.
- Elemento: Talio
- Símbolo: Tl
- Periodo: 6
- Grupo: 13
- Número atómico: 81
- Orbitales para: z = 81: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p1.
- Orbitales para: z = 81: [Xe], 6s2, 4f14, 5d10, 6p1.
- Elemento: Plomo
- Símbolo: Pb
- Periodo: 6
- Grupo: 14
- Número atómico: 82
- Orbitales para: z = 82: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p2.
- Orbitales para: z = 82: [Xe], 6s2, 4f14, 5d10, 6p2.
- Elemento: Bismuto
- Símbolo: Bi
- Periodo: 6
- Grupo: 15
- Número atómico: 83
- Orbitales para: z = 83: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p3.
- Orbitales para: z = 83: [Xe], 6s2, 4f14, 5d10, 6p3.
- Elemento: Polonio
- Símbolo: Po
- Periodo: 6
- Grupo: 16
- Número atómico: 84
- Orbitales para: z = 84: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p4.
- Orbitales para: z = 84: [Xe], 6s2, 4f14, 5d10, 6p4.
- Elemento: Astato
- Símbolo: At
- Periodo: 6
- Grupo: 17
- Número atómico: 85
- Orbitales para: z = 85: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p5.
- Orbitales para: z = 85: [Xe], 6s2, 4f14, 5d10, 6p5.
- Elemento: Radón
- Símbolo: Rn
- Periodo: 6
- Grupo: 18
- Número atómico: 86
- Orbitales para: z = 86: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6.
- Orbitales para: z = 86: [Rn].
- Elemento: Francio
- Símbolo: Fr
- Periodo: 7
- Grupo: 1
- Número atómico: 87
- Orbitales para: z = 87: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s1.
- Orbitales para: z = 87: [Rn], 7s1.
- Elemento: Radio
- Símbolo: Ra
- Periodo: 7
- Grupo: 2
- Número atómico: 88
- Orbitales para: z = 88: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2.
- Orbitales para: z = 88: [Rn], 7s2.
- Elemento: Actinio
- Símbolo: Ac
- Periodo: 7
- Grupo:
- Número atómico: 89
- Orbitales para: z = 89: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2,
5f1. - Orbitales para: z = 89: [Rn], 7s2,
5f1.
- Excepción: 16. Promoción de un electrón de 5f a 6d.
- Orbitales para: z = 89: [Rn], 7s2, 5f0, 6d1.
- Elemento: Torio

- Símbolo: Th
- Periodo: 7
- Grupo:
- Número atómico: 90
- Orbitales para: z = 90: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2,
5f2. - Orbitales para: z = 90: [Rn], 7s2,
5f2.
- Excepción: 17. Promoción de dos electrones de 5f a 6d.
- Orbitales para: z = 90: [Rn], 7s2, 5f0, 6d2.
- Elemento: Protactinio

- Símbolo: Pa
- Periodo: 7
- Grupo:
- Número atómico: 91
- Orbitales para: z = 91: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2,
5f3. - Orbitales para: z = 91: [Rn], 7s2,
5f3.
- Excepción: 18. Promoción de un electrón de 5f a 6d.
- Orbitales para: z = 91: [Rn], 7s2, 5f2, 6d1.
- Elemento: Uranio

- Símbolo: U
- Periodo: 7
- Grupo:
- Número atómico: 92
- Orbitales para: z = 92: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2,
5f4. - Orbitales para: z = 92: [Rn], 7s2,
5f4.
- Excepción: 19. Promoción de un electrón de 5f a 6d.
- Orbitales para: z = 92: [Rn], 7s2, 5f3, 6d1.
- Elemento: Neptunio

- Símbolo: Np
- Periodo: 7
- Grupo:
- Número atómico: 93
- Orbitales para: z = 93: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2,
5f5. - Orbitales para: z = 93: [Rn], 7s2,
5f5.
- Excepción: 20. Promoción de un electrón de 5f a 6d.
- Orbitales para: z = 93: [Rn], 7s2, 5f4, 6d1.
- Elemento: Plutonio
- Símbolo: Pu
- Periodo: 7
- Grupo:
- Número atómico: 94
- Orbitales para: z = 94: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f6.
- Orbitales para: z = 94: [Rn], 7s2, 5f6.
- Elemento: Americio
- Símbolo: Am
- Periodo: 7
- Grupo:
- Número atómico: 95
- Orbitales para: z = 95: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f7.
- Orbitales para: z = 95: [Rn], 7s2, 5f7.
- Elemento: Curio

- Símbolo: Cm
- Periodo: 7
- Grupo:
- Número atómico: 96
- Orbitales para: z = 96: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2,
5f8. - Orbitales para: z = 96: [Rn], 7s2,
5f8.
- Excepción: 21. Promoción de un electrón de 5f a 6d.
- Orbitales para: z = 96: [Rn], 7s2, 5f7, 6d1.
- Elemento: Berkelio
- Símbolo: Bk
- Periodo: 7
- Grupo:
- Número atómico: 97
- Orbitales para: z = 97: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f9.
- Orbitales para: z = 97: [Rn], 7s2, 5f9.
- Elemento: Californio
- Símbolo: Cf
- Periodo: 7
- Grupo:
- Número atómico: 98
- Orbitales para: z = 98: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f10.
- Orbitales para: z = 98: [Rn], 7s2, 5f10.
- Elemento: Einsteinio
- Símbolo: Es
- Periodo: 7
- Grupo:
- Número atómico: 99
- Orbitales para: z = 99: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f11.
- Orbitales para: z = 99: [Rn], 7s2, 5f11.
- Elemento: Fermio
- Símbolo: Fm
- Periodo: 7
- Grupo:
- Número atómico: 100
- Orbitales para: z = 100: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f12.
- Orbitales para: z = 100: [Rn], 7s2, 5f12.
- Elemento: Mendelevio
- Símbolo: Md
- Periodo: 7
- Grupo:
- Número atómico: 101
- Orbitales para: z = 101: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f13.
- Orbitales para: z = 101: [Rn], 7s2, 5f13.
- Elemento: Nobelio
- Símbolo: No
- Periodo: 7
- Grupo:
- Número atómico: 102
- Orbitales para: z = 102: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14.
- Orbitales para: z = 102: [Rn], 7s2, 5f14.
- Elemento: Laurencio
- Símbolo: Lr
- Periodo: 7
- Grupo: 3
- Número atómico: 103
- Orbitales para: z = 103: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14,
6d1. - Orbitales para: z = 103: [Rn], 7s2, 5f14,
6d1.
- Excepción: 22. Promoción de un electrón de 6d a 7p.
- Orbitales para: z = 103: [Rn], 7s2, 5f14, 6d0, 7p1.
- Elemento: Rutherfordio
- Símbolo: Rf
- Periodo: 7
- Grupo: 4
- Número atómico: 104
- Orbitales para: z = 104: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d2.
- Orbitales para: z = 104: [Rn], 7s2, 5f14, 6d2.
- Elemento: Dubnio
- Símbolo: Db
- Periodo: 7
- Grupo: 5
- Número atómico: 105
- Orbitales para: z = 105: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d3.
- Orbitales para: z = 105: [Rn], 7s2, 5f14, 6d3.
- Elemento: Seaborgio
- Símbolo: Sg
- Periodo: 7
- Grupo: 6
- Número atómico: 106
- Orbitales para: z = 106: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d4.
- Orbitales para: z = 106: [Rn], 7s2, 5f14, 6d4.
- Elemento: Bohrio
- Símbolo: Bh
- Periodo: 7
- Grupo: 7
- Número atómico: 107
- Orbitales para: z = 107: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d5.
- Orbitales para: z = 107: [Rn], 7s2, 5f14, 6d5.
- Elemento: Hassio
- Símbolo: Hs
- Periodo: 7
- Grupo: 8
- Número atómico: 108
- Orbitales para: z = 108: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d6.
- Orbitales para: z = 108: [Rn], 7s2, 5f14, 6d6.
- Elemento: Meitnerio
- Símbolo: Mt
- Periodo: 7
- Grupo: 9
- Número atómico: 109
- Orbitales para: z = 109: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d7.
- Orbitales para: z = 109: [Rn], 7s2, 5f14, 6d7.
- Elemento: Darmstadtio
- Símbolo: Ds
- Periodo: 7
- Grupo: 10
- Número atómico: 110
- Orbitales para: z = 110: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d8.
- Orbitales para: z = 110: [Rn], 7s2, 5f14, 6d8.
- Elemento: Roentgenio
- Símbolo: Rg
- Periodo: 7
- Grupo: 11
- Número atómico: 111
- Orbitales para: z = 111: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d9.
- Orbitales para: z = 111: [Rn], 7s2, 5f14, 6d9.
- Elemento: Copernicio
- Símbolo: Cn
- Periodo: 7
- Grupo: 12
- Número atómico: 112
- Orbitales para: z = 112: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10.
- Orbitales para: z = 112: [Rn], 7s2, 5f14, 6d10.
- Elemento: Nihonio
- Símbolo: Nh
- Periodo: 7
- Grupo: 13
- Número atómico: 113
- Orbitales para: z = 113: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p1.
- Orbitales para: z = 113: [Rn], 7s2, 5f14, 6d10, 7p1.
- Elemento: Flerovio
- Símbolo: Fl
- Periodo: 7
- Grupo: 14
- Número atómico: 114
- Orbitales para: z = 114: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p2.
- Orbitales para: z = 114: [Rn], 7s2, 5f14, 6d10, 7p2.
- Elemento: Moscovio
- Símbolo: Mc
- Periodo: 7
- Grupo: 15
- Número atómico: 115
- Orbitales para: z = 115: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p3.
- Orbitales para: z = 115: [Rn], 7s2, 5f14, 6d10, 7p3.
- Elemento: Livermorio
- Símbolo: Lv
- Periodo: 7
- Grupo: 16
- Número atómico: 116
- Orbitales para: z = 116: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p4.
- Orbitales para: z = 116: [Rn], 7s2, 5f14, 6d10, 7p4.
- Elemento: Teneso
- Símbolo: Ts
- Periodo: 7
- Grupo: 17
- Número atómico: 117
- Orbitales para: z = 117: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p5.
- Orbitales para: z = 117: [Rn], 7s2, 5f14, 6d10, 7p5.
- Elemento: Oganesón
- Símbolo: Og
- Periodo: 7
- Grupo: 18
- Número atómico: 118
- Orbitales para: z = 118: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p6, 5s2, 4d10, 5p6, 6s2, 4f14, 5d10, 6p6, 7s2, 5f14, 6d10, 7p6.
- Orbitales para: z = 118: [Og].
Excepciones al Diagrama de Moeller
De la 22 excepciones conocidas al Diagrama de Moeller, que se producen en unos casos muy específicos,
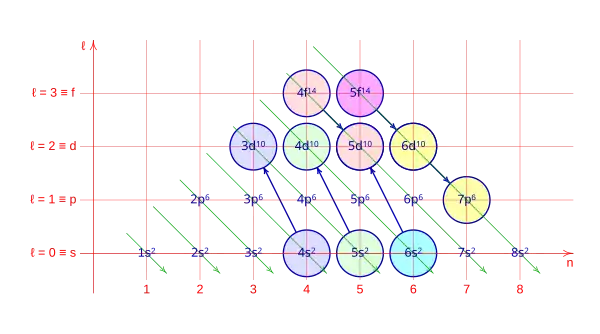
Donde podemos diferenciar tres casos:
La promoción s → d: 4s → 3d, 5s → 4d, 6s → 5d.
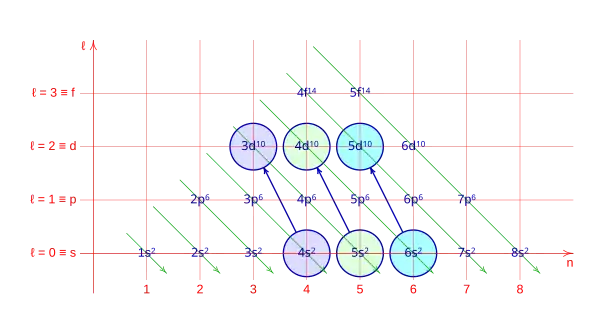
La promoción f → d: 4f → 5d, 5f → 6d.
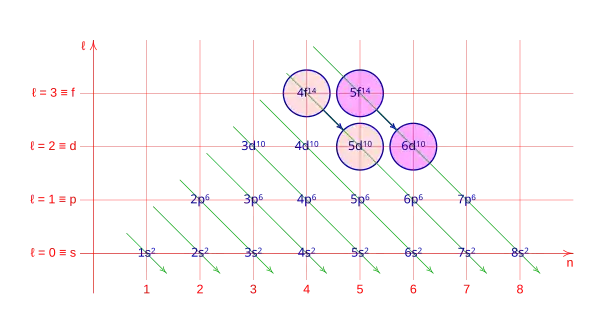
Y la promoción 6d → 7p, del cual solo hay un caso.

Ver la tabla periódica
La promoción de electrones: 4s → 3d
| Elemento | Símbolo | N. atómico | Periodo | Grupo | Ot | Or |
|---|---|---|---|---|---|---|
| Cromo | Cr | 24 | 4 | 6 | [Ar], |
[Ar], 4s1, 3d5. |
| Níquel | Ni | 28 | 4 | 10 | [Ar], 4s2, 3d8. | [Ar], 4s1, 3d9. |
| Cobre | Cu | 29 | 4 | 11 | [Ar], |
[Ar], 4s1, 3d10. |
La promoción de electrones: 5s → 4d.
| Elemento | Símbolo | N. atómico | Periodo | Grupo | Ot | Or |
|---|---|---|---|---|---|---|
| Niobio | Nb | 41 | 5 | 5 | [Kr], |
[Kr], 5s1, 4d4. |
| Molibdeno | Mo | 42 | 5 | 6 | [Kr], |
[Kr], 5s1, 4d5. |
| Tecnecio | Tc | 43 | 5 | 7 | [Kr], |
[Kr], 5s1, 4d6. |
| Rutenio | Ru | 44 | 5 | 8 | [Kr], |
[Kr], 5s1, 4d7. |
| Rodio | Rh | 45 | 5 | 9 | [Kr], |
[Kr], 5s1, 4d8. |
| Paladio | Pd | 46 | 5 | 10 | [Kr], |
[Kr], 5s0, 4d10. |
| Plata | Ag | 47 | 5 | 11 | [Kr], |
[Kr], 5s1, 4d10. |
La promoción de electrones: 6s → 5d.
| Elemento | Símbolo | N. atómico | Periodo | Grupo | Ot | Or |
|---|---|---|---|---|---|---|
| Platino | Pt | 78 | 6 | 10 | [Xe], |
[Xe], 6s1, 4f14, 5d9. |
| Oro | Au | 79 | 6 | 11 | [Xe], |
[Xe], 6s1, 4f14, 5d10. |
La promoción de electrones: 4f → 5d.
| Elemento | Símbolo | N. atómico | Periodo | Grupo | Ot | Or |
|---|---|---|---|---|---|---|
| Lantano | La | 57 | 6 | [Xe], 6s2, |
[Xe], 6s2, 4f0, 5d1. | |
| Cerio | Ce | 58 | 6 | [Xe], 6s2, |
[Xe], 6s2, 4f1, 5d1. | |
| Gadolinio | Gd | 64 | 6 | [Xe], 6s2, |
[Xe], 6s2, 4f7, 5d1. |
La promoción de electrones: 5f → 6d.
| Elemento | Símbolo | N. atómico | Periodo | Grupo | Ot | Or |
|---|---|---|---|---|---|---|
| Actinio | Ac | 89 | 7 | [Rn], 7s2, |
[Rn], 7s2, 5f0, 6d1. | |
| Torio | Th | 90 | 7 | [Rn], 7s2, |
[Rn], 7s2, 5f0, 6d2. | |
| Protactinio | Pa | 91 | 7 | [Rn], 7s2, |
[Rn], 7s2, 5f2, 6d1. | |
| Uranio | U | 92 | 7 | [Rn], 7s2, |
[Rn], 7s2, 5f3, 6d1. | |
| Neptunio | Np | 93 | 7 | [Rn], 7s2, |
[Rn], 7s2, 5f4, 6d1. | |
| Curio | Cm | 96 | 7 | [Rn], 7s2, |
[Rn], 7s2, 5f7, 6d1. |
Promoción de electrones: 6d → 7p.
| Elemento | Símbolo | N. atómico | Periodo | Grupo | Ot | Or |
|---|---|---|---|---|---|---|
| Laurencio | Lr | 103 | 7 | 3 | [Rn], 7s2, 5f14, |
[Rn], 7s2, 5f14, 6d0, 7p1. |
Bibliografía
- Edwin M. Larsen (1972). Elementos de Transicion (Juan Mª Salietti Vinué, trad.). Editorial Reverté, S.A.
- Leslie E. Orgel (1964). Introducción a la química de los metales de transición. Editorial Reverté. ISBN 978-84-291-9189-9.
Referencias
- ↑ Desmond Grosvenor Cooper (1976). La tabla periódica (José Gálvez Flores, trad.). Reverté. ISBN 97-884-291-7138-9.
- ↑ Richard E. Dickerson; Harry B. Gray; Marcetta Y. Darensbourg; Donald J. Darensbourg (1992). «8». Principios de química (José Gálvez Flores, trad.) (3 edición). Reverté. p. 303. ISBN 97-884-291-7175-4.
- ↑ Ira N. Levine (2001). Química cuántica (Alberto Requena Rodríguez, trad.) (5 edición). Pearson Educación. ISBN 97-884-205-3096-3.