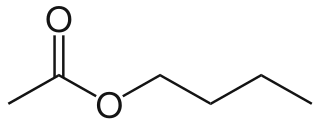
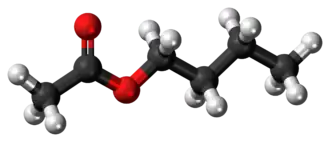
Acetato de butilo
| Acetato de n-butilo | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| Butil acetato | ||
| General | ||
| Otros nombres |
Éster butílico Etanoato de butilo | |
| Fórmula semidesarrollada |
CH 3COO(CH 2) 3CH 3 | |
| Fórmula molecular | C6H12O2 | |
| Identificadores | ||
| Número CAS | 123-86-4[1] | |
| Número RTECS | AF7350000 | |
| ChEBI | 31328 | |
| ChEMBL | CHEMBL284391 | |
| ChemSpider | 29012 | |
| PubChem | 31272 | |
| UNII | 464P5N1905 | |
| KEGG | C12304 | |
|
CCCCOC(=O)C
| ||
| Propiedades físicas | ||
| Apariencia | Líquido incoloro | |
| Olor | Frutal | |
| Densidad | 880 kg/m³; 0,88 g/cm³ | |
| Masa molar | 116,2 g/mol | |
| Punto de fusión | −78 °C (195 K) | |
| Punto de ebullición | 126,1 °C (399 K) | |
| Presión de vapor | 1.2 kPa (20 °C) | |
| Viscosidad | 0.685 cP (25 °C) | |
| Conductividad térmica | 0.136 W/m·K (25 °C) | |
| Constante de Henry (kH) | 0.281 L·atm/mol | |
| Propiedades químicas | ||
| Solubilidad en agua | 5,3 g/l (20 °C) | |
| Momento dipolar | 1.87 (24 °C) D | |
| log P | 1.82 | |
| Termoquímica | ||
| ΔfH0gas | −609.6 kJ/mol | |
| Capacidad calorífica (C) | 3467 kJ/mol | |
| Peligrosidad | ||
| SGA |
  | |
| Punto de inflamabilidad | 310 K (37 °C) | |
| NFPA 704 |
3
2
0
| |
| Temperatura de autoignición | 633 K (360 °C) | |
| Frases H | H226 H336 HEUH066 | |
| Límites de explosividad | 1,2 - 7,5 (%vol) | |
| Riesgos | ||
| Riesgos principales | Es inflamable y relativamente volátil | |
| Ingestión | Puede provocar dolor abdominal, pesadez, náusea, vómitos y debilidad | |
| Inhalación | Puede causar náuseas, anemia, alteraciones hepáticas y del sistema nervioso central | |
| Piel | Provoca un efecto desengrasante en la piel produciendo enrojecimiento, descamación y fisuras. | |
| Ojos | Puede causar enrojecimiento, dolor y visión borrosa | |
| LD50 | 10768 mg/kg (ratas, oral) | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El acetato de n-butilo es un compuesto orgánico con fórmula CH
3COO(CH
2)
3CH
3. Es el éster derivado del n-butanol y el ácido acético. Es un líquido incoloro e inflamable, que se encuentra en muchas frutas, a las que confiere sabores característicos y un olor dulzón a plátano o manzana. Se usa ampliamente como disolvente industrial, solo o combinado con otros compuestos orgánicos (comúnmente xileno o tolueno).[2]
Existen tres isómeros del acetato de n-butilo (cuatro, si incluimos estereoisómeros), que son acetato de isobutilo, acetato de ter-butilo y acetato de sec-butilo (con dos enantiómeros).
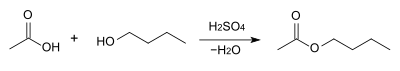
Producción y usos
El acetato de butilo se fabrica habitualmente a mediante la esterificación de Fischer del butanol (o sus isómeros, para obtener el éster isómero correspondiente) y ácido acético, en presencia de ácido sulfúrico:[2]
El acetato de butilo se utiliza principalmente como disolvente para resinas sintéticas,[3] pinturas y tintas.[2] Es un componente de la laca de uñas.[4] Debido a su gran poder disolvente, el acetato de butilo, es muy utilizado en las industrias de tintas y barnices y muchos tipos de revestimientos y acabados. También como ingrediente de sabores y esencias frutales. Se utiliza también en la fabricación de lacas, plásticos, películas fotográficas, y cueros artificiales. [3]
Peligrosidad
En cuanto a la peligrosidad, su punto de inflamación está en 295 K (22 °C), y su temperatura de autoignición en 633 K (360 °C). Sus vapores forman con el aire mezclas inflamables o explosivas a temperatura ambiente. Irrita las mucosa y sistema respiratorio, piel y ojos, produciendo daño en los tejidos y conjuntivitis en los ojos. Los efectos narcóticos de acetato de n-butilo es mayor que los ésteres de alquilo. También, las toxicidades y acciones irritantes son algo mayor que isopropilo, y acetatos de etilo.[3]
Presencia en la naturaleza
El sabor de las manzanas, especialmente en la variedad 'Red Delicious', se debe en parte a este compuesto. Las feromonas de alarma emitidas por la glándula de Koschevnikov de las abejas contiene acetato de butilo.
Referencias
- ↑ Número CAS
- ↑ a b c Ullmann's encyclopedia of industrial chemistry. Wiley-VCH. 2010. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a01_045.
- ↑ a b c «Disolventes en la Industria Química/Ésteres».
- ↑ Schneider, Günther; Gohla, Sven; Schreiber, Jörg; Kaden, Waltraud; Schönrock, Uwe; Schmidt-Lewerkühne, Hartmut; Kuschel, Annegret; Petsitis, Xenia; Pape, Wolfgang; Ippen, Hellmut; Diembeck, Walter (2001). «Skin Cosmetics». Ullmann's Encyclopedia of Industrial Chemistry. ISBN 3527306730. doi:10.1002/14356007.a24_219.
Enlaces externos
 Wikimedia Commons alberga una categoría multimedia sobre Acetato de butilo.
Wikimedia Commons alberga una categoría multimedia sobre Acetato de butilo.- Ethylene and other chemicals in fruit
- Material Safety Data Sheet
- CDC - NIOSH Pocket Guide to Chemical Hazards